上報 Up Media
toggle- 最新消息 陳昭如:男人組內閣,女人生小孩 2024-04-19 00:02
- 最新消息 快訊/台北市停電「東區772戶」黑漆漆 恐要等凌晨才能恢復 2024-04-18 22:44
- 最新消息 【花蓮7.2強震】台積電災損發重訊 估Q2「認列損失30億」 2024-04-18 22:29
- 最新消息 【415限電危機】台電「1度砸12元」向請民間發電 台積電未簽約仍可獲補償 2024-04-18 22:25
- 最新消息 遭控收賄17億 中國央行前副行長范一飛當庭認罪 2024-04-18 21:55
- 最新消息 好噁!桃園知名燒臘店驚見活蛆蠕動 衛生局稽查14項缺失 2024-04-18 21:45
- 最新消息 【廢死論辯】「殺人償命還錢天經地義」 犯保協會鑑定報告:判死對家屬是安慰 2024-04-18 21:45
- 最新消息 【415限電危機】王美花稱事前沒聽說消息 藍委秀台電內部訊息怒轟 2024-04-18 21:40
- 最新消息 《Garena 傳說對決》推出「五五好團節」改版 「魔法連環戰」刺激登場 2024-04-18 21:02
- 最新消息 【有片】 德軍新型榴彈發射器標案 奧地利史泰爾GL40拿下首張歷史性訂單 2024-04-18 21:00
美國消費者有越來越多的藥物來自中國,但中國製造的藥品卻問題橫生。(湯森路透)
中國身為「世界工廠」,但是其品質管理卻是令人心驚膽戰,尤其是「救命藥」。彭博社(Bloomberg)今年出報導「受污染的中國製造心臟藥如何躲過美國食品藥品監督管理局(FDA)的稽查」,帶出整個藥物供應鍊所出現的「藥命」危機。甚至用下圖插圖,來諷刺中國「學名藥」廠的可怕品質。
 (圖片擷取自Bloomberg網頁)
(圖片擷取自Bloomberg網頁)
其實,這不是新聞。去年,FDA發出警告:目前數百萬美國所服用的中國製的心臟藥被化學物質污染,有致癌的風險。
故事是發生在2017年,有位FDA檢查員隨機抽查中國製藥商浙江華海製藥有限公司(Zhejiang Huahai Pharmaceutical Co. Ltd.)竟然在官方記錄上「忘記」檢測結果。但其實這不是偶然,再深入調查發現該廠設施和設備老舊沒有維修,沒有調查前的測試結果就已經異常,更可怕的是,「未知的雜質」竟然被視為數值錯誤而被忽略。所以,他向這家製藥廠同時也是中國最大的藥品出口商之一發出警告,如果該廠無法釐清問題,他們無法生產新的學名藥。

結果,這位檢查員的決定被他的頂頭上司駁回。FDA竟然允許華海自動自發解決問題。原因是該廠一直「以來合乎規定」的表現,以及認定該廠已經對測試中的「雜質」反應充分(adequate responses)。這件事,後來被媒體發現,FDA的名譽掃地。FDA一開始還死不認錯,在公開聲明說「在常規檢查。不可能召回藥品源頭來控制危害」
這藥物得安穩(Diovan)是常用於治療高血壓和心臟衰竭,來自浙江華海的特定纈沙坦(valsartan)已被一種已知的致癌物質N-亞硝基二甲胺(NDMA)污染。受污染藥物可能造成肝臟損害(纖維化,瘢痕形成,肝功能異常測試)以及腎臟和肝臟腫瘤(惡性和良性腫瘤)FDA在2018年夏天緊急召回這批受污染的藥品。整件事美國民眾憤怒的是,FDA「慢好幾拍」的守舊作法使美國民眾暴露在風險中。
不過,冤有頭債有主,中國製藥廠要負很大的責任。FDA要華海「自己改善」問題。很不幸,該廠還是我行我素,再次發現NDMA的蹤跡是來自另一個華海的下游客戶。這顯示,浙江華海完全不當一回事,那是什麼原因使浙江華海一錯再錯呢?
回溯一下,纈沙坦的歷史。瑞士製藥廠諾華(Novartis AG)看中高血壓患者大約數十億的需求,開發活性成分纈沙坦,並在1996年上市得安穩(Diovan)。美國專利於2012年到期,浙江華海爭取到這天大的學名藥機會。因為要出口到美國市場,必須通過FDA的批准。但因為浙江華海透過「善巧」方式,他們只需要提供FDA藥物主要成分,而不用匯報製藥過程的變化。壞就壞在這裡,浙江華海在其中,動了至關重要的「手腳」。
華海更改了溶劑,他們使用與諾華不同的溶劑。華海的溶劑選擇是二甲基甲酰胺或二甲基甲酰胺,他們在中國申請專利時大言不慚是「增加效率,易於控制雜質」。但華海副董事長終於承認最重要的原因是「省錢」。這讓華海的價格可以比主要的印度競爭對手低10%,一舉擴大全球市佔額。也正是這樣的「便宜」改變使該藥物有NDMA的雜質,讓多數的病患有致癌的風險。雖然他對美國人民是「無良」的存在,卻是中共的「優秀資產」。
浙江華海創辦人陳保華,卻被授與「優秀共產黨員」、「優秀企業家」、「突出貢獻經營者」,現為人大代表、政協委員。這在廣大受害人眼中卻是格外的諷刺,利潤是來自於病患的「性命」。不只如此,中國政府以行動完全挺華海。從2018年8月到10月,臨海市政府向華海捐贈了3億元「工業發展援助資金」。去年12月,華海贏得了六項政府招標,在11個城市提供低成本學名藥。華海1月份表示,希望通過私募基金方式籌募18億人民幣,為研發中心提供資金,以及「智能製造」計畫。即使知道華海作法有問題,中國政府沒有半句苛責,反而呵護有加。似乎,中國對於自己企業,已經到了不論是非的「溺愛」程度了。
華海草菅人命的態度固然「該死」,但如果在往上推想,這其實是結構的「共業」。不論是現任川普政府,以及所有民主黨都支持「政治正確」的口號:降低美國的藥價。
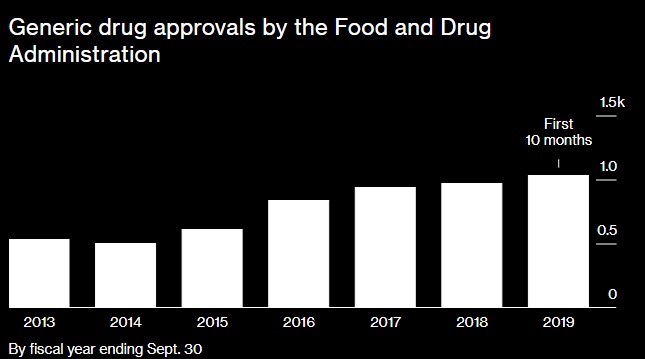
今年七月,川普發佈行政命令要使美國藥價降至全世界最低。那些藥廠當然會把這「業果」回給消費者。因為要便宜,所以在很久以前,FDA增加逐年增加「較便宜」的海外學名藥的批准。現在,美國消費者有越來越多的藥物來自中國,因為生產成本比較低。根據統計,中國製造的藥物在2018年至10月30日期間佔FDA通用批准的8%,高於2015年的1%。(如下圖所示)
過去,FDA的藥物批准程序建立在信任的基礎上,特別是對製造商的信任。現在,美國製藥有85%位於海外,中國和印度佔多數,但是中國跟印度政府的「監督標準」卻沒那麼嚴格。FDA原本的基礎是「信任」,但是當地政府的標準罄竹難書,FDA吃不消這麼龐大的業務。即使,2016年當川普第一次喊出「降低」常備藥價格時,FDA發下豪願要強化其海外稽查能力,作為總統宏願的一環。但是,這樣工作光靠「願力」是不夠的,客觀環境的難為。
FDA「方便」隨機抽查美國國內廠商,即使如此,根據FDA統計,去年也才抽查五分之一。姑且不論,FDA無法如此頻繁抽查海外工廠。再加上,國外與本國不同,必須「事先告知」對方才能進行調查。又受限語言障礙及造訪時間有限。即使FDA檢查員非常「努力」跟上外國藥品製造商的步伐,這些製造商還會掩蓋其生產中的問題。種種因素,使FDA在中國的檢查能量無法持久。(如下圖所示)
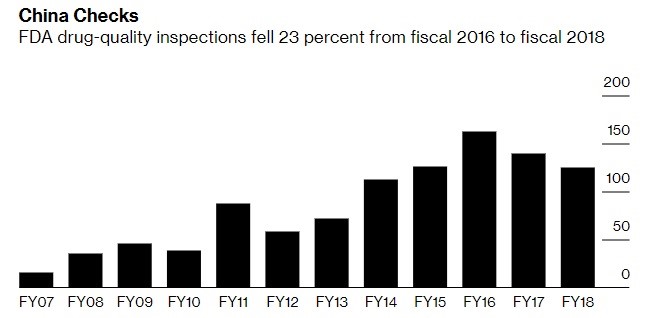
華海的案件,提醒了FDA確實在監察藥物市場的必須克服挑戰,藥物越來越多外包給海外,大多流向中國。這也揭發美國依賴其他國家製造「常備藥」的脆弱性。
黑斯廷斯中心(The Hastings Center)的醫療專家羅斯瑪麗吉布森(Rosemary Gibson)去年出版「中國製藥:揭露美國對中國製藥的依賴風險」(China Rx: Exposing the Risks of America's Dependence on China for Medicine)在書中,她估計美國學名藥及非處方藥80%的成分都來自中國或印度。當川普在關稅與中國「貿易戰」下,「食物(農產品)被當作戰爭武器,藥物也可以成為對付美國的武器」吉布森如是說。現在,中國已經緊緊掐住了美國的脖子,不用開槍,就可以取美國人的性命吉布森在書中說,「美國市場很容易受到中國受污染產品的影響」
美國在「政治正確」下,要求降低藥廠藥價,在價格競爭機制之下,使美國的患者多使用中國或印度的學名藥,或是從中國進口製藥原料。這已經把美國自己脖子洗乾淨,把刀子親自「交給」中國。在中國甚至還沒自己意會到自己手握「致命武器」前,中國廠商被「營利」蒙蔽了良知,使百萬的美國患者染上致癌的風險,就已經可能「害死」大量美國人。FDA扛下所有的監察責任,但是,防不慎防,心有餘力而不足,今日華海案也只是被發現的冰山一角。
「中國製造」的悲劇不停在上演,因果循環,美國,最終,自己害死了自己的人民。
※作者台大博士/旅美學人
熱門影音
熱門新聞
- 《淚之女王》金智媛、金秀賢互飆演技收視破20% 「洪海仁墓碑」劇照瘋傳網憂BE結局
- 《蓮花樓》成毅新劇高馬尾造型曝光帥翻 憑2關鍵奪回藝名聲勢輾壓師兄任嘉倫
- 【《承歡記》內幕曝光】楊紫片酬拿2億演技卻被罵翻 許凱演霸總9千萬輕鬆入袋
- 《與鳳行》林更新公開女友惹怒CP粉 趙麗穎親上火線17字幫忙救場超暖心
- 【韓星片酬大公開】金秀賢拍《淚之女王》因「這理由」降價演出 IU身價輾壓宋慧喬
- 肖戰新劇凝視《惜花芷》張婧儀畫面曝光甜出汁 新片與《在暴雪時分》趙今麥演兄妹超吸睛
- 白敬亭拍趙露思《偷偷藏不住》姐妹作制服照曝光 「這關鍵」帥度不敵陳哲遠
- 《你也有今天》陳星旭新劇抱迪麗熱巴畫面曝光 1關鍵CP感完勝她與《在暴雪時分》吳磊