上報 Up Media
toggle- 最新消息 何清漣專欄:川普內閣成員的對中態度──原則與靈活兼備 2024-12-12 07:00
- 最新消息 李濠仲專欄:蔣萬安忘了上海不准布拉格和台北友好 2024-12-12 07:00
- 最新消息 中共挑釁「新常態」 台灣國防「新對策」 2024-12-12 07:00
- 最新消息 檢方第9度提訊!被問不法所得是否上億 柯文哲未回應 2024-12-11 22:35
- 最新消息 【大法官人事案】難忘被害人家屬絕望神情 王碧芳:我支持死刑 2024-12-11 22:16
- 最新消息 法總理上任僅3個月垮台 馬克宏擬48小時內提新人選 2024-12-11 21:56
- 最新消息 動輒飆罵下屬「混蛋」 數發部2主管涉霸凌降調非主管職務 2024-12-11 21:51
- 最新消息 南韓總統辦公室僅提交小部分資料 警方搜查行動無功而返 2024-12-11 21:28
- 最新消息 陸委會「有條件」放行雙城論壇 北市府:秉持4原則持續交流 2024-12-11 21:14
- 最新消息 【大法官人事案】反對翁曉玲版《憲訴法》 王碧芳:會癱瘓憲法法庭 2024-12-11 20:45
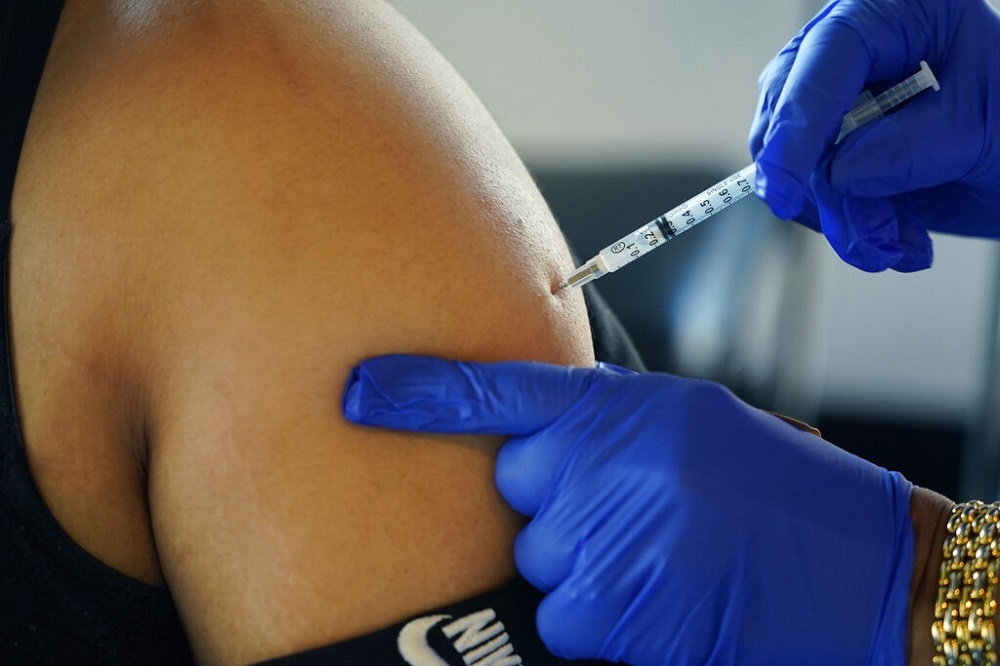
美國FDA批准輝瑞和莫德納的雙價疫苗加強劑。(資料照片/美聯社)
美國食品藥物管理局(FDA)8月31日批准輝瑞BNT和莫德納的雙價疫苗用作單劑的加強劑,這兩支疫苗皆可對抗原始的新冠病毒,以及Omicron的亞變種株BA.4和BA.5。
根據FDA新聞稿,莫德納的雙價加強劑獲批准用於18歲以上的成人,輝瑞的雙價加強劑則適用於12歲以上,施打資格皆為已完整接種任何獲批准的新冠疫苗或加強劑,達兩個月以上者。
FDA OKs OMICRON BOOSTER SHOTS: Updated COVID-19 boosters from Pfizer and Moderna have been given emergency use authorization by the FDA. The boosters are redesigned vaccines targeting omicron and the BA.4 and BA.5 subvariants. @ErielleReshef has details. https://t.co/Sbmuo9v8iJ pic.twitter.com/zuhIcMuysL
— World News Tonight (@ABCWorldNews) September 1, 2022
(延伸閱讀:美FDA建議10月開打新一輪追加劑 新疫苗瞄準Omicron變異株對症下藥)
新聞稿指出,現階段美國的新冠案例多為BA.4和BA.5,且秋冬疫情料將繼續擴散;此前,FDA的專家小組曾於6月底召開會議,決議疫苗加強劑應針對Omicron調整設計。FDA局長克里夫(Robert M. Califf)表示,疫苗加強劑拯救無數性命,有助於減少重症風險,呼籲符合資格的民眾施打雙價加強劑,增強自身免疫力。
FDA批准之後,仍需美國疾病管制暨預防中心(CDC)的顧問小組提出建議及CDC主任瓦倫斯基(Rochelle Walensky)放行;該顧問小組將於9月1日召開會議,就輝瑞和莫德納的雙價疫苗加強劑展開討論。
7月底,美國衛生部宣布已向莫德納訂購6600萬劑雙價加強劑;此前,當局亦向輝瑞訂了1.05億劑雙價疫苗,總計約有1.71億劑雙價加強劑可用來因應秋冬疫情。不過,此數量並不足以讓每一位美國人都接種;衛生部指出,美國政府跟輝瑞和莫德納的合約中,各包含再追加3億劑訂單的選擇權。
據美聯社報導,輝瑞稱到下周結束前,預計可出貨1500萬劑;莫德納則僅稱「接下來幾天」將可出貨。不過,目前僅有33%的美國人施打過加強劑,比例並不高,因此接下來還有多少美國人願意再捲起袖子接種,是一大考驗。
路透則指出,這批疫苗很可能是最後一批免費提供給美國人的新冠疫苗;8月底,美國衛生部應急處置助理部長歐康納(Dawn O'Connell)表示,拜登政府可能於明年1月時用盡採購、配送新冠疫苗的聯邦資金,而政府的目標是將提供新冠疫苗和治療藥物的重擔,透過「審慎、協調好」的方式,逐步轉移至市場機制運作。









